同源康医药CDK2/4/6抑制剂TYK-0540片I期临床研究首例受试者入组
发布时间:2024年01月04日
2024年01月02日,同源康医药宣布,其自主研发的新一代口服、高效小分子CDK2/4/6抑制剂TYK-0540片I期临床研究项目(登记号CTR20233663)在中国科学技术大学附属第一医院(安徽省立医院)完成首例受试者入组。
本研究包括剂量递增和扩展入组两部分,由复旦大学附属肿瘤医院张剑教授牵头,旨在评估TYK-0540片在局部晚期/转移性实体瘤患者中安全性和耐受性,确定最大耐受剂量(MTD),并评估初步疗效。

吴豫生博士
同源康医药董事长吴豫生博士表示:“我们一直在寻求新疗法的开发,以改善恶性肿瘤患者的生存和生活治疗。TYK-0540在临床前研究中展示出较好的抗肿瘤效应和安全性。本例受试者入组示TYK-0540在中国首例入组,这将是一项重大里程碑事件”。
关于CDK2/4/6
细胞周期蛋白依赖性激酶(Cyclin-dependent kinases, CDKs)是一组丝氨酸/苏氨酸激酶,其催化活性可以受到细胞周期蛋白与CDK抑制剂的调节。CDK具有调节细胞周期检查点和DNA转录的作用,被认为是细胞分裂增殖过程中一类关键性调控因子[1]。已有研究证明CDK1、2、3、4、6直接作用于细胞周期转换和细胞分裂行为,而CDK7-11调节DNA转录[1]。
临床研究已经证实CDK4/6抑制剂在激素受体阳性HER-2受体阴性乳腺癌的治疗中获得了超越标准疗法的生存获益。尽管CDK4/6抑制剂极大的改变了HR+/HER2-乳腺癌的治疗格局,但仍存在巨大的挑战,主要表现为CDK4/6抑制剂的原发和获得性耐药。在使用CDK4/6抑制剂治疗的患者中约有20%的患者表现为起始治疗无效即原发性耐药,另有一半在25个月内发展为耐药并疾病进展[2]。
研究发现当CDK4/6活性被抑制后,随着Cyclin E的扩增以及MYC的激活,MYC上调激活CDK2,CDK2-CyclinE可以作为代偿性途径使Rb磷酸化,释放E2F,促使肿瘤细胞增殖,这是CDK4/6抑制剂获得性耐药的主要机制[3]。Cyclin E过表达使肿瘤细胞抵抗CDK4/6的抑制作用,不再停滞于G1期[4]。有研究显示Cyclin E高表达患者对CDK4/6抑制剂不敏感,其无进展生存期明显短于Cyclin E扩增引起的耐药,该机制已经在CDK4/6耐药细胞系中得到确认[5]。想要达到长期的疗效,CDK4和CDK2都需要被抑制,这是一种新的抑制癌细胞的治疗方式。同时靶向CDK2/4/6有望减少CDK4/6抑制耐药的发生。
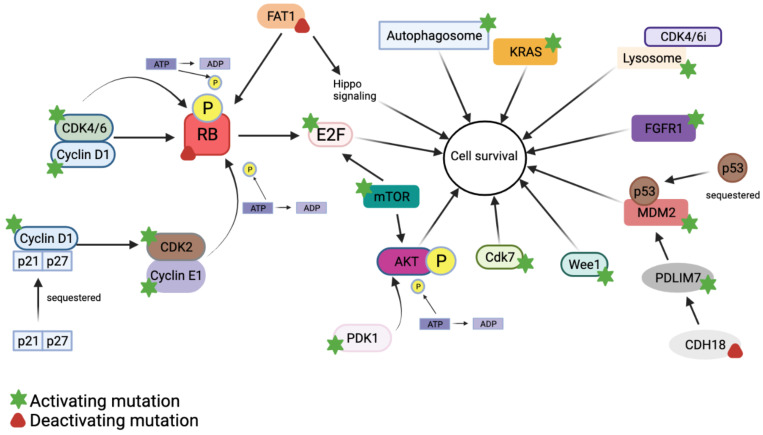
CDK4/6抑制剂耐药机制
参考文献:
[1]. Ding L, Cao J, Lin W, et al. The Roles of Cyclin-Dependent Kinases in Cell-Cycle Progression and Therapeutic Strategies in Human Breast Cancer. Int J Mol Sci. 2020;21(6):1960. Published 2020 Mar 13. doi:10.3390/ijms21061960.
[2]. Goetz MP, Toi M, Campone M, et al. MONARCH 3: Abemaciclib As Initial Therapy for Advanced Breast Cancer. J Clin Oncol. 2017;35(32):3638-3646. doi:10.1200/JCO.2017.75.6155.
[3]. Freeman-Cook K, Hoffman RL, Miller N, et al. Expanding control of the tumor cell cycle with a CDK2/4/6 inhibitor. Cancer Cell. 2021;39(10):1404-1421.e11. doi:10.1016/j.ccell.2021.08.009.
[4]. Freeman-Cook KD, Hoffman RL, Behenna DC, et al. Discovery of PF-06873600, a CDK2/4/6 Inhibitor for the Treatment of Cancer. J Med Chem. 2021;64(13):9056-9077. doi:10.1021/acs.jmedchem.1c00159.
[5]. O’Leary B, Finn RS, Turner NC. Treating cancer with selective CDK4/6 inhibitors. Nat Rev Clin Oncol. 2016;13(7):417-430. doi:10.1038/nrclinonc.2016.26.
